[2026-01-30] (Accès libre) Swissmedic, l’Institut suisse des produits thérapeutiques, a publié le 30 janvier 2026 les résultats de d’une campagne ciblée de surveillance du marché réalisée auprès des importateurs.
Contexte
Swissmedic surveille le marché des dispositifs médicaux de manière ciblée et examine chaque année certains thèmes prioritaires sur le marché suisse, allant des opérateurs économiques aux dispositifs eux-mêmes. L’objectif de ces campagnes ciblées est de sensibiliser les opérateurs économiques à leurs obligations.
Les thèmes des campagnes ciblées sont définis en tenant notamment compte des retours issus de la surveillance nationale et internationale du marché, des signalements reçus, ainsi que du contexte réglementaire.
Résultats de la campagne réalisée
Entre mars et novembre 2025, une campagne ciblée a été menée auprès des importateurs, sur des produits couramment utilisés tels que les cathéters, les canules, les instruments chirurgicaux et les instruments de diagnostic.
Swissmedic a ainsi inspecté 30 importateurs et a testé 232 échantillons de produits.
Les résultats de la campagne synthétisés sur 1 page montrent que pour 57 % des importateurs des écarts ont été constatés portant sur :
- la vérification des dispositifs,
- de leurs informations accompagnant les dispositifs,
- et des conditions de stockage et de transport.
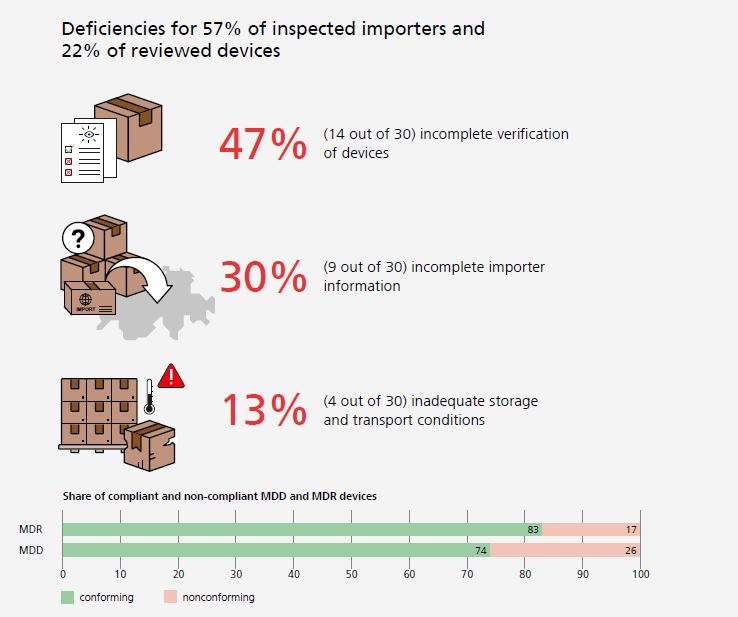
Illustration des résultats obtenus
En comparaison avec la campagne ciblée menée en 2023, les améliorations sont mineures. Par conséquent et au vu des résultats obtenus, les activités de surveillance du marché se poursuivront auprès des importateurs.
Conclusion
Cette approche démontre que non seulement les fabricants peuvent être inspectés, mais aussi les importateurs. Ces derniers font partie intégrante de la chaîne logistique des dispositifs médicaux et peuvent avoir un impact potentiel sur ceux-ci. Cette démarche s’inscrit dans une dynamique globale et internationale visant à renforcer la maîtrise et la surveillance des opérateurs économiques afin de garantir la sécurité des patients.
Article rédigé par Lam-Xé NOEL, Directrice Générale de DM Experts SAS
