[2024-03-06] (Accès libre) La Commission européenne vient de publier une mise à jour de la liste des normes harmonisées à l’appui du règlement (UE) 2017/746 relatif aux dispositifs médicaux de diagnostic in vitro (RDMDIV).
La décision d’exécution (UE) 2024/817 vient donc amender la décision d’exécution (UE) 2021/1195. Comme indiqué dans le titre de la dernière décision d’exécution, les nouvelles normes harmonisées au RDMDIV sont relatives à « la stérilisation des produits de santé et aux emballages des dispositifs médicaux stérilisés au stade terminal » et sont présentées dans le détail dans le tableau suivant :
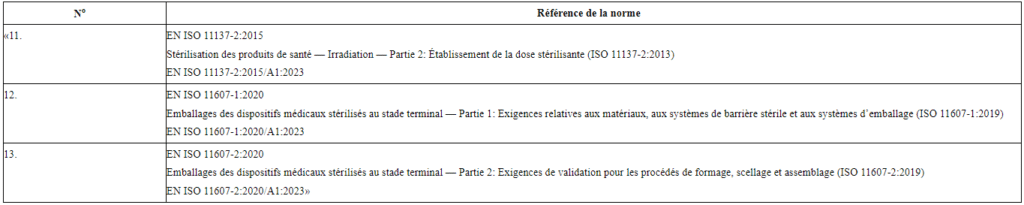
Aucune norme figurant dans la version antérieure de la liste n’a été modifiée ou retirée.
Pour mémoire, la liste complète des normes harmonisées au RDMDIV est disponible sur le site de la Commission européenne, au format PDF (uniquement en anglais) ou au format MS Excel (en plusieurs langues, dont le français), selon vos préférences.
Article rédigé par Audrey GILBERT, membre du réseau DM Experts.
