[2025-12-08] (Accès libre) Quasiment 1 an après un communiqué de presse virulent, publié par le SNITEM, concernant le cadre du projet de loi de financement de la sécurité sociale (PLFSS) 2025, un nouveau communiqué au titre alarmant a été émis : « PLFSS pour 2026 : le gouvernement sacrifie les PME de la Medtech ».
Contexte
Le PLFSS pour 2026 a été présenté en Conseil des ministres le 14 octobre 2025, puis adopté le 16 décembre 2025. Le gouvernement a voté un abaissement supplémentaire du seuil de la clause de sauvegarde 2026 fixé pour 2026 à 2,19 milliards d’euros (article L. 138-19-8 du code de la sécurité sociale). Pour comparaison, le seuil pour 2024 avait déjà été réduit à 2,26 milliards d’euros, contre 2,31 milliards précédemment.
Cette modification législative entraînerait une charge fiscale supplémentaire d’environ 150 millions d’euros pour les entreprises du secteur des dispositifs médicaux, en particulier les PME implantées sur les territoires français.
Contenu du communiqué
Le communiqué accuse le gouvernement, lors du vote du PLFSS à l’Assemblée nationale en nouvelle lecture, d’avoir choisi de « sacrifier » les PME de la Medtech en adoptant cet abaissement, malgré les alertes formulées par le rapporteur du PLFSS à l’Assemblée nationale, le député Thibault Bazin.
Le SNITEM souligne que :
- l’impact est particulièrement fort dans les territoires, menaçant la capacité d’innovation, les emplois et la vitalité d’un écosystème stratégique pour la santé publique ;
- les PME représentent environ 70 % des entreprises supportant cette charge fiscale dans le secteur des dispositifs médicaux.
Le syndicat dénonce également que cette décision :
- n’établit pas de dialogue et est imposée de manière unilatérale,
- contraste avec d’autres sujets où des concertations avaient été jugées productives, par exemple sur la prise en charge des fauteuils roulants.
Le communiqué se termine par un appel au Parlement pour accompagner le secteur et soutenir les entreprises concernées afin de limiter les effets négatifs de cette mesure.
Entreprises adhérentes du SNITEM concernées
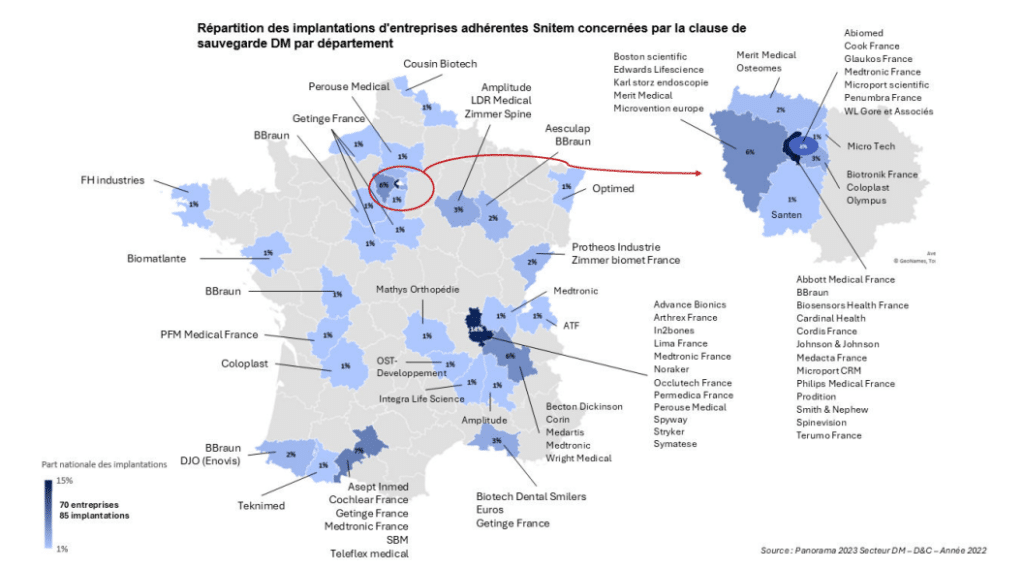
Illustration tirée du communiqué de presse du SNITEM
Une infographie du SNITEM présente la liste des entreprises concernées et leur localisation, avec des chiffres concrets alarmants. À titre d’exemple, pour une PME « type » du secteur des dispositifs médicaux implantables (37 salariés, forte activité de R&D) : le déclenchement de la clause pourrait représenter jusqu’à 25 % de sa masse salariale annuelle ou 35 % de son budget de recherche à reverser à l’État en une seule fois. À l’échelle nationale, ce sont 10 000 emplois directs, des centres de recherche et des sites industriels entiers qui sont exposés à un risque réel d’affaiblissement.
Conclusion
On peut légitimement se poser la question : quelle place la France souhaite-t-elle accorder à son industrie des dispositifs médicaux ? À force de considérer ce secteur comme une variable d’ajustement budgétaire, le risque est de fragiliser durablement un écosystème pourtant stratégique pour les patients, l’innovation et l’emploi.
Article rédigé par Lam-Xé NOEL, Directrice Générale de DM Experts SAS
