[2025-03-20] (Accès libre) L’ANSM (Agence nationale de sécurité du médicament et des produits de santé) a publié le 20 mars 2025 un guide sur la gestion des signalements de matériovigilance, réactovigilance et des avis de sécurité en établissements de santé.
Ce guide a été rédigé par un groupe de travail informel constitué par : l’ANSM, les coordonnateurs régionaux de matériovigilance et de réactovigilance (CRMRV), les correspondants locaux de matériovigilance et de réactovigilance, ainsi que des représentants des entreprises françaises du secteur des dispositifs médicaux (DM) et des dispositifs médicaux de diagnostic in vitro (DMDIV).
Pour mémoire, la matériovigilance et la réactovigilance sont des systèmes de surveillance visant à détecter, évaluer et prévenir les incidents liés aux DM et aux DMDIV. L’Union européenne a renforcé ces obligations avec les règlements (UE) 2017/745 et (UE) 2017/746, imposant aux fabricants, professionnels de santé et établissements de signaler tout incident susceptible de compromettre la sécurité des patients.
Objectif
Ce guide de 33 pages, intitulé « Guide Gestion des signalements de matériovigilance, réactovigilance et des avis de sécurité en établissements de santé » vise à standardiser les procédures de gestion des incidents, assurer une réaction rapide et harmonisée, et renforcer la communication entre les différents acteurs. Il précise le rôle des fabricants et autres opérateurs économiques, établissements de santé et autorités de régulation dans le signalement et le suivi des incidents.
Champ d’application
Ce guide s’adresse aux :
- professionnels de santé utilisant des DM et DMDIV ;
- correspondants locaux de matériovigilance et réactovigilance (CLMV/CLRV) des établissements de santé ;
- opérateurs économiques : fabricants, mandataires, distributeurs, importateurs et assembleurs de dispositifs médicaux ;
- autorités de régulation telles que l’ANSM ;
- responsables qualité et gestionnaires de risques au sein des établissements de santé.
Présentation des principaux chapitres du document
Préambule, définitions et introduction
- précision des termes clés : matériovigilance (MV), réactovigilance (RV), dispositif médical (DM), dispositif de diagnostic in vitro (DMDIV), action corrective de sécurité (FSCA), avis de sécurité (FSN) ;
- importance de la surveillance des DM et DMIV ;
- références réglementaires principales ;
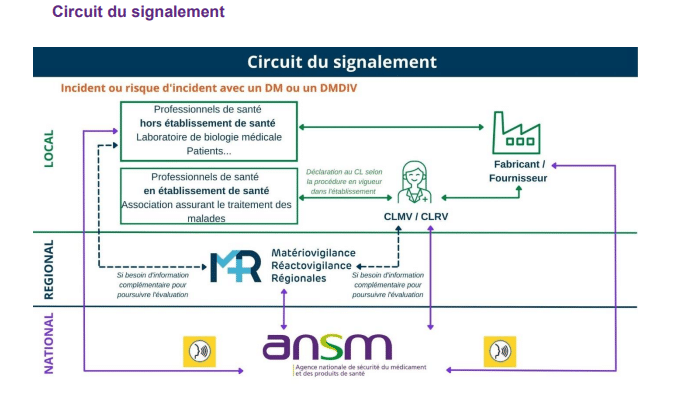
- circuit du signalement : schéma de circulation de l’information entre les professionnels de santé, le correspondant local de vigilance (CLMV/CLRV), l’ANSM et les fabricants ;
- rappel des obligations des opérateurs économiques fournisseurs de DM et DMDIV aux établissements de santé ;
- processus de traitement d’un signalement de vigilance par un opérateur économique ;
- rappel des obligations des établissements de santé ;
- processus de traitement d’un incident par le correspondant local de matériovigilance ou de réactovigilance de l’établissement de santé.
Identification d’un incident de matério- ou réactovigilance :
- reconnaissance des événements indésirables potentiels ;
- liste des informations à fournir, classification selon la gravité et le risque pour les patients ;
- vérification de la récidivité ou de précédents signalements, identification.
Signalement (à l’ANSM et aux fournisseurs de dispositifs) :
- notification obligatoire pour tout incident grave ou récurrent, risques d’incident grave,… ;
- canaux et formulaires de signalement officiels ;
- délais réglementaires de transmission.
Analyses et investigations :
- conservation et récupération du dispositif ;
- évaluation technique et clinique de l’incident ;
- identification des facteurs contributifs ;
- collaboration entre l’établissement de santé et le fabricant.
Transmission des conclusions :
- rédaction d’un rapport final détaillé ;
- communication des résultats aux parties prenantes ;
- proposition de mesures correctives ou préventives.
Cas des actions correctives de sécurité (FSCA) et de la transmission des avis de sécurité (FSN) :
- définition et objectifs des FSCA et FSN ;
- rôles et responsabilités des fabricants et distributeurs ;
- communication des FSN aux utilisateurs et autorités de santé
- mise en œuvre des mesures correctives de sécurité :
- planification et suivi des actions correctives ;
- vérification de la bonne application des recommandations ;
- documentation et traçabilité des actions.
Liens :
- ressources et contacts pour déclarer les incidents ;
- accès aux plateformes de signalement réglementaires.
Conclusion
Ce document propose un cadre opérationnel structurant la gestion des incidents et des avis de sécurité. Il favorise une réaction rapide et une amélioration continue de la sécurité des DM et DIV dans les établissements de santé. Il insiste sur la nécessité d’une coordination renforcée entre tous les acteurs du système de santé pour garantir la sécurité des dispositifs médicaux et de leurs utilisateurs.
Article rédigé par Audrey Gilbert, membre du réseau DMEXPERTS
