[2026-03-23] (Accès libre) Le MDCG (groupe de coordination des dispositifs médicaux) a publié, en mars 2026, la 1re révision du guide MDCG 2025-8 pour la définition de l’identifiant unique (Master UDI-DI) pour les montures de lunettes, les verres de lunettes, et les lunettes de lecture prémontées.
Pour ces catégories de dispositifs, dits « hautement individualisés », le « Master UDI-DI » permet de regrouper des dispositifs qui partagent une même combinaison de paramètres de conception, définis dans le règlement délégué (UE) 2025/1920.
Ce guide très complet de 44 pages s’intitule : « MDCG 2025-8 Rev.1 – Guidance on the implementation of the Master UDI-DI solution for spectacle frames, spectacle lenses and ready-to-wear reading spectacles ». Nous vous avions présenté son contenu dans un article précédent du réseau DMEXPERTS.
Contenu de la révision
Les modifications sont mineures. Elles permettent de corriger des coquilles qui s’étaient introduites dans des schémas concernant les verres ophtalmiques (spectacles lenses).
Les voici résumées visuellement ci-dessous.
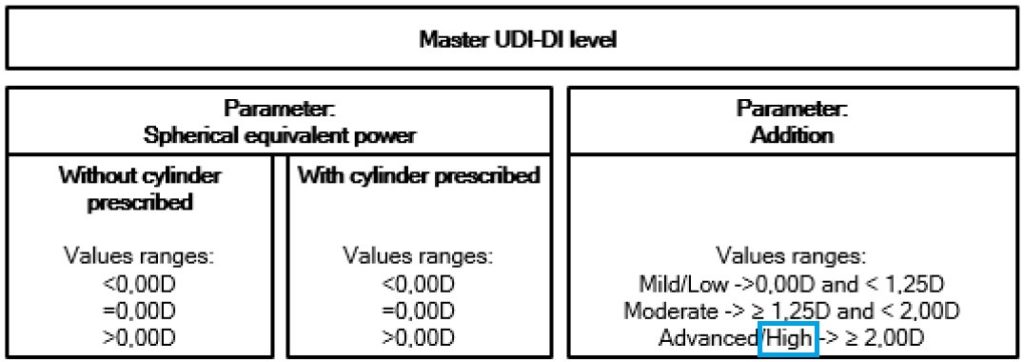
Contenu de la modification 1 : schéma d’attribution
Contenu de la modification 2 : arbre de décision « example#2 »

Conclusion
Dorénavant, partout dans le document, le groupe de plage d’addition supérieure à 2 dioptries correspond au groupe de déficience visuelle presbytie « Avancée/Élevée » (« Advanced/High »).
Remercions pour leur rigueur les auteurs de ce guide remarquable.
Enfin, si vous vous interrogez sur le planning de mise en œuvre du Master UDI-DI, vous pouvez consulter notre dernier article sur le sujet.
Article rédigé par Muriel GONIDEC, Présidente de DM Experts SAS