[2024-11-20] (Accès libre) L’ANSM (agence nationale de sécurité du médicament et des produits de santé) a publié le 20 novembre 2024 le compte rendu du Comité Scientifique Permanent « Surveillance DM et DMDIV » du 11 mars 2024.
Pour mémoire, ce comité a pour mission de veiller à la qualité du système de surveillance du marché, de proposer des stratégies, des enquêtes nationales et des mesures à prendre en matière de matériovigilance et de réactovigilance.
Cette séance avait comme ordre du jour :
- Introduction
- Surveillance des marchés des DM
- Circuits pour circulation extracorporelle (CEC) et oxygénation par membrane extracorporelle (ECMO)
- Étude sur les capuchons imprégnés
- Mobile de radiologie FRD Nano
- Cas marquants : définition et mode opératoire
- Tour de table des cas marquants
- Point divers
Ce compte rendu de 11 pages présente, après un bref rappel du contexte réglementaire, plusieurs « cas marquants » concernant des dispositifs médicaux (DM) et des dispositifs médicaux de diagnostic in vitro (DMDIV), ainsi qu’une proposition de prise en charge des « cas marquants » par les coordinateurs régionaux de matériovigilance et de réactovigilance (CRMRV).
Ce dernier point est celui ayant retenu notre attention et sera développé dans cet article :
En premier lieu, le « cas marquant » a été redéfini et ne concerne pas seulement les cas de matériovigilance et réactovigilance observés.
En second lieu, un logigramme de prise en charge a été proposé et explicité :
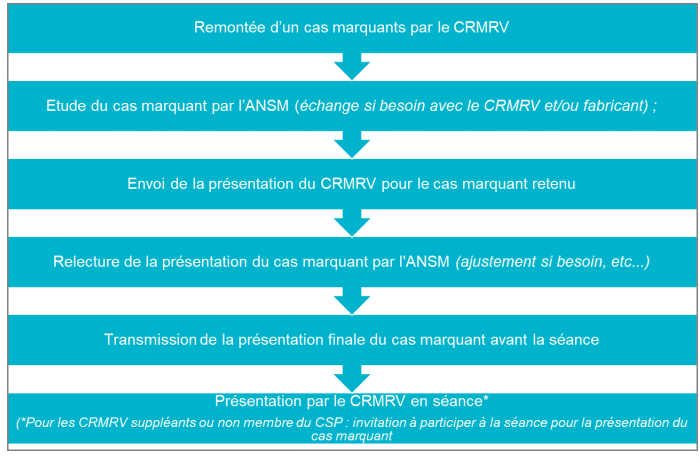
Les autres points abordés concernent des DM et DMDIV particuliers, et nous vous invitons à lire les passages vous intéressant dans ce compte rendu. Ils concernent :
- les circuits pour circulation extracorporelle (CEC) et oxygénation par membrane extracorporelle (ECMO) ;
- la perméabilité des valves bidirectionnelles à l’isopropanol des capuchons désinfectants ;
- un mobile de radiologie portable ;
- l’avis de sécurité concernant les respirateurs d’anesthésie ;
- un point sur les cas d’enfants retrouvés contre le plexiglas de la couveuse en dehors du matelas (Incubateur fermé) ;
- un cas de décès lors de l’utilisation du ciment chirurgical ;
- la difficulté de mettre en œuvre l’action corrective sur des insufflateurs ;
- un point de suivi sur la décision de police sanitaire relative aux dispositifs de perfusion.
Article rédigé par Audrey Gilbert, membre du réseau DMEXPERTS
